マイランEPD合同会社(本社:東京都港区、社長:本田明彦、以下「マイランEPD」)は、慢性便秘症治療薬「アミティーザカプセル12μg」(一般名:ルビプロストン)の製造販売承認を本日9月21日に取得いたしましたのでお知らせします。本剤は、本年11月の薬価収載ならびに発売を予定しています。
慢性便秘症は、日常的によくみられる疾患ですが、患者さんのQOLを著しく低下させる軽視できない症状です。また、加齢とともに男女ともに患者数が増加することから、超高齢社会を迎える日本では注目が高まっています。
慢性便秘症*治療薬「アミティーザ」は、ClC-2クロライドチャネルを活性化することにより腸管内の水分分泌を促し、自然な排便を促す薬剤として、2012年11月に24μgカプセル製剤の販売を開始しました。昨年10月に刊行された『慢性便秘症診療ガイドライン2017』**では、アミティーザを含む上皮機能変容薬は、推奨の強さ1(合意率98%)、エビデンスレベルAと高い評価を得ています。
今回、「アミティーザカプセル24μg」の半分の含有量である12μgの規格追加により、慢性便秘症患者さん、特に高齢の慢性便秘症患者さんへ長期投与する際に用量調整がしやすくなり、副作用の軽減ならびに服薬アドヒアランスの向上に対する寄与が期待されています。
これについて横浜市立大学医学部 肝胆膵消化器病学 主任教授の中島淳氏は『慢性便秘症の患者さんは症状や病態が様々です。そういった患者さんの治療において、用量調節の選択肢が増えることは望ましいと考えています』と述べています。
マイランEPDでは、アミティーザを通して、1人でも多くの慢性便秘症患者さんに貢献できるよう、引き続き取り組んでまいります。
*器質的疾患による便秘を除く
**日本消化器病学会関連研究会慢性便秘の診断・治療研究会,南江堂,東京, 2017
(参考)
原因が特定できない慢性便秘症患者を対象としたルビプロストンカプセルの自発排便回数の変化量に基づく同等性の確認について
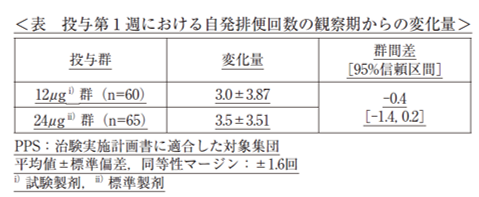
自発排便回数が平均 3 回/週未満の状態が 6 ヵ月以上持続している慢性便秘症の患者を対象に,12μg(試験製剤)群は 1 回12μgカプセルを 2 カプセルずつ、24μg(標準製剤)群は 1 回24μgカプセルを 1 カプセルずつ、 1 日 2 回朝夕食後に 7 日間投与した。主要評価項目である投与第 1 週における自発排便回数の観察期からの変化量は以下の表のとおりであり、95%信頼区間は事前に設定した同等性マージンの範囲内であった。
マイランについて
マイランは世界中で事業を展開する医薬品企業であり、ヘルスケア分野で新しいスタンダードを確立するために全力で取り組んでいます。世界70億の人々に高品質な医薬品をお届けし、 革新的な技術でアンメットニーズにお応えすることを実現します。常に高い信頼性と卓越したサービスを目指し、安易なことではなく正しいことを行い、熱意あふれるグローバル・リーダーシップを 発揮して未来を切り開きます。世界中で7500以上の製品を提供しており、抗レトロウィルス医薬品については世界でHIVエイズ患者の約40%に使用されています。約165の国と地域で製品を販売し、 世界最大級の規模で医薬品原料を製造しています。35,000人を超える社員は、“健康でより良い世界を創る”ことに専心しています。詳細はmylan.comをご覧ください。
日本では、マイラン製薬株式会社がジェネリック医薬品のリーディングカンパニーとして、マイランEPD合同会社が消化器疾患、呼吸器疾患、アレルギー疾患、感染症領域、 ウイメンズヘルスの領域を中心に事業を展開しています。www.mylan.co.jp








































